智能化可控释放纳米递药系统可以对pH、温度、光照、氧化剂、酶以及超声辐照等外界情形的刺激做出反响性响应��,并依附其优异的控制释放功效��,在药物传输系统中体现出极具竞争力的应用远景��。其该系统可针对肿瘤细胞与正常组织的生物学差别选择性释药��,从而有用降低抗肿瘤药物对正常细胞的毒副作用��,提高药物的使用率��。但由于肿瘤组织及细胞的情形重大性��,简单刺激模式或者简朴的功效输出已不可知足聚合物质料的需求��。因此��,生长新型刺激条件、多元化刺激方法和具有逻辑控制特点的功效响应成为修建刺激响应性聚合物系统研究的焦点所在��。
中国科学院成都生物研究所李帮经课题组致力于基于环糊精主客体识别作用来修建智能纳米递药系统研究��。针对肿瘤细胞内保存的高浓度谷胱甘肽(GSH)及酸性情形特征��,该课题组使用环糊精修饰的自然多糖透明质酸和金刚烷修饰的抗癌药物喜树碱(ADA-CPT)��,通过环糊精与金刚烷的特异性主客体识别作用��,简朴高效地修建了一类双重肿瘤微情形刺激响应性纳米递药系统��。在纳米药物载体通过肿瘤组织的EPR作用富集在肿瘤组织中��,并进一步被肿瘤细胞内吞后��,肿瘤细胞内酸性情形将环糊精与透明质酸相连的pH敏感的亚胺键破损��,释放出环糊精与金刚烷的包合物(β-CD/ADA-CPT)��,形成粒径更小的载药纳米体�����;同时��,在高浓度的GSH情形下��,ADA-CPT分子中的双硫键结构破损��,进一步释放出抗癌药物CPT��,实现对肿瘤细胞的杀灭作用��。通过使用肿瘤细胞内的酸性情形及高浓度GSH情形��,该双重刺激响应性的纳米递药系统还可以实现抗癌药物的分步按需释放��,提供更为灵巧的控制释放性能��。
 ?
?
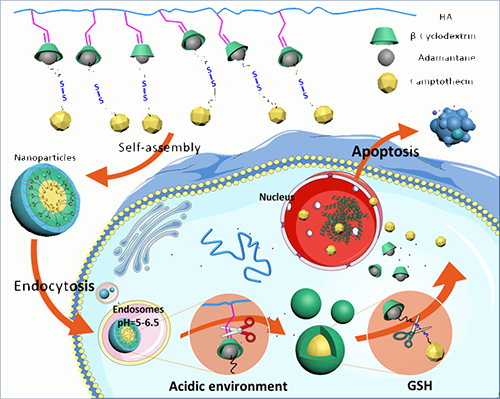
pH、GSH双重刺激响应性纳米药物载体的自组装及肿瘤细胞内释药示意图
相关研究效果揭晓在Polymer Chemistry上��。(pH, glutathione dual-triggered supramolecular assemblies as synergistic and controlled drug release carrier. Polymer Chemistry, 2017, DOI: 10.1039/C7PY01644A)��。论文的第一作者为中科院成都生物所助理研究员康洋��。
论文链接:http://pubs.rsc.org/en/content/articlelanding/2017/py/c7py01644a#!divAbstract